| ที่มา | มติชนสุดสัปดาห์ ฉบับวันที่ 22 - 28 มีนาคม 2567 |
|---|---|
| คอลัมน์ | ทะลุกรอบ |
| ผู้เขียน | ดร. ป๋วย อุ่นใจ |
| เผยแพร่ |
ทะลุกรอบ | ป๋วย อุ่นใจ
เทคโนโลยีอัณฑะจิ๋วกู้โลก…
ในช่วงนี้ วงการเนื้อสัตว์เพาะเลี้ยงและวิศวกรรมเนื้อเยื่อของอิสราเอลกำลังครึกครื้น
เพราะนอกจากข่าวอเล็ปฟาร์มส์ (Aleph Farms) บริษัทเทคโนโลยีการเกษตรระดับเซลล์เจ้าดังจากดินแดนศักดิ์สิทธิ์ที่ตัดสินใจจับมือกับสตาร์ตอัพสายเทคจากแดนภารตะอย่าง “เฟิร์มบ๊อกซ์ไบโอ (Fermbox Bio)” และพันธมิตรสัญชาติไทยอย่างบีบีจีไอ (BBGI) เตรียมเปิดโรงงานเนื้อสัตว์เพาะเลี้ยง (cultured meat) ในไทยแบบยิ่งใหญ่อลังการจนสะท้านสะเทือนไปทั่วในวงการอุตสาหกรรมอาหาร
แต่ในฝากฝั่งวิจัยการแพทย์ ก็ไม่น้อยหน้า เพราะงานวิจัยสุดพิสดาร “สู่อัณฑะเพาะเลี้ยง : การสร้างออร์แกนอยด์อัณฑะหนูที่มีโครงสร้างและองค์ประกอบเหมือนอัณฑะจริง (Towards a “Testis in a Dish” : Generation of Mouse Testicular Organoids that Recapitulate Testis Structure and Expression Profiles)” ที่เพิ่งตีพิมพ์ออกมาในวารสาร International Journal of Biological Sciences ของนิตเซน โกเนน (Nitzen Gonen) นักวิจัยนาโนเทคโนโลยีและวัสดุศาสตร์จากมหาวิทยาลัยบาร์ อิลาน (Bar Ilan University) ในประเทศอิสราเอล พิลึกพิลั่นเสียจนกลายเป็นข่าวโด่งดังให้ผู้คนโจษขานกันไม่แพ้ข่าว “สเต๊กจากหลอดทดลองของอเล็ปฟาร์มส์”
เปเปอร์ออกมาปั๊บ เรื่องราวของ “อัณฑะจิ๋วเลี้ยงในแล็บ” ก็กลายเป็นข่าวดังพาดหัวปั๊บ…ก็ชื่อเปเปอร์จัดเต็ม เรียกทัวร์เสียขนาดนั้น ถ้าผู้คนจะไม่ฮือฮาสิแปลก
คำถามคือความคิดอะไรอยู่ในหัวของนิตเซน ทำไมเธอถึงเลือกที่จะหาวิธีเพาะเลี้ยงอัณฑะ?
คงไม่ใช่ว่าอยากเอาไปปรุงเมนูเปิบพิสดารหรือเอามาเป็นวัตถุดิบขันแข่งในรายการสารพัดเชฟเป็นแน่…
และสิ่งที่เธอบอกก็คือ “เพราะว่าอยากจะรู้และเข้าใจได้ว่าอสุจินั้นสร้างขึ้นมาได้อย่างไรอย่างถ่องแท้”
นิตเซนเผยว่าปัญหาการมีบุตรยากนั้นส่งผลกระทบอย่างมากในสังคม ในชายหนุ่มวัยฉกรรจ์สิบคน อย่างน้อยหนึ่งคนจะมีปัญหากับการสร้างทายาทสืบต่อวงศ์ตระกูล…ซึ่งเป็นประเด็นใหญ่มากในสังคมโลก โดยเฉพาะอย่างยิ่งในปัจจุบันที่อัตราการเกิดของเด็กรุ่นใหม่ในหลายประเทศลดน้อยลงจนน่าตกใจ…
ปัญหายิ่งใหญ่ขนาดนี้ แน่นอนว่าต้องมีคนสนใจอยู่ไม่น้อย ทีมอิสราเอลไม่ใช่ทีมแรกและไม่ใช่ทีมเดียวที่พยายามจะสร้างอสุจิในหลอดทดลอง
ในประวัติศาสตร์ เทคโนโลยีเพาะเลี้ยงอัณฑะในหลอดทดลองนั้นเกิดขึ้นครั้งแรกตั้งแต่ช่วงปี 1920 ในประเทศฝรั่งเศส ในตอนนั้น นักชีววิทยา ซีเอช แชมปี (CH Champy) พยายามที่จะหากรรมวิธีที่จะรักษาสภาพชิ้นส่วนเนื้อเยื่อของอัณฑะกระต่ายให้อยู่รอดให้ได้นานที่สุด
เขาตัดสินใจเอาชิ้นอัณฑะกระต่ายไปเพาะเลี้ยงในพลาสมา (ส่วนใสของเลือด) และผลที่ได้ก็เกินคาด เพราะนอกจากชิ้นอัณฑะจะอยู่รอดได้เป็นสัปดาห์แล้ว อัณฑะกระต่ายของเขานั้นยังสามารถสร้างเซลล์ตัวอ่อนของอสุจิที่เรียกว่า “สเปิร์มมาโตไซต์ (spermatocyte)” ออกมาได้อีกด้วย
ในตอนนั้นการค้นพบของแชมปีเป็นอะไรที่ว้าวมากในวงการวิจัยระบบสืบพันธุ์เพศชาย และเริ่มดึงดูดความสนใจของทีมวิจัยจากทั่วทุกสารทิศ
ต่อในช่วงยุคซิกตี้ วงการเพาะเลี้ยงอัณฑะก็เริ่มบูม…
ผู้คนมากมายเริ่มหันมาสนใจปัญหาแห่งเพศชาย ในช่วงนั้น เทคโนโลยีการกล่อมเกลี้ยงเลี้ยงดูอสุจิมากมายถูกพัฒนาขึ้นมาอย่างรวดเร็ว
ความก้าวหน้าด้านงานวิจัยเซลล์สืบพันธุ์พุ่งทะยานราวกับติดจรวด
ทว่า พอเริ่มทดลองจะเอาไปใช้จริง หลายเทคโนโลยีกลับให้ผลออกมากลับตาลปัตร
กระบวนการสร้างอสุจิในสิ่งมีชีวิต (spermatogenesis) นั้นเป็นกระบวนการที่ซับซ้อนถึงขีดสุด มีการเปลี่ยนแปลงหลายขั้นหลายตอนในระดับเซลล์ ซึ่งยากมากที่จะติดตามจนรู้ชัดว่าเกิดอะไรขึ้นบ้าง แค่ที่รู้กันในตอนนี้ ก็ทำเอาหลายคนมึนไปหลายตลบแล้ว
โดยทั่วไปก็คือกระบวนการนี้เริ่มต้นจากเซลล์ตั้งต้นของอสุจิที่เรียกว่าสเปิร์มาโตโกเนียม (spermatogonium) พัฒนาต่อไปเป็นเซลล์ตัวอ่อนของอสุจิที่เรียกว่า “สเปิร์มมาโตไซต์ปฐมภูมิ (Primary spermatocyte)” หลังจากนั้น เซลล์สเปิร์มมาโตไซต์ปฐมภูมิก็จะแบ่งเซลล์แบบไมโอสิส (Meiosis) รอบแรกเพื่อลดจำนวนชุดโครโมโซมและเพิ่มจำนวนเซลล์จนได้เป็นเซลล์ตัวอ่อนอสุจิที่เรียกว่าสเปิร์มมาโตไซต์ทุติยภูมิ (Secondary spermatocyte) สองเซลล์ และจะแบ่งต่อไมโอสิสในรอบที่สองจนได้เป็นเซลล์ตัวอ่อนอสุจิที่เรียกว่าสเปิร์มมาติด (Spermatid) จำนวนสี่เซลล์
ท้ายที่สุด เซลล์ตัวอ่อนสเปิร์มมาติดจะพัฒนาต่อไปเป็นอสุจิเต็มวัย หรือที่เรียกว่า “สเปิร์มมาโตซัว (spermatozoa)” ซึ่งอสุจิเต็มวัยนี้เอง ที่เหล่านักวิจัยอยากที่จะสร้างได้…
แต่ทว่า ด้วยความซับซ้อนของกระบวนการสร้างอสุจิ แม้ว่าจะมีเทคโนโลยีมากมายถูกพัฒนาขึ้นมาเพื่อการเพาะเลี้ยงอสุจิ ตั้งแต่การพัฒนาสูตรอาหารเหลวเพื่อเลี้ยงชิ้นส่วนหรือเซลล์อัณฑะ (cultivation of dissociated testicular cells or testis fragment) การเลี้ยงเซลล์ในโครงร่างสามมิติให้พัฒนาออกมาเป็นออร์แกนอยด์อัณฑะจิ๋ว (3D testicular organoid culture) ไปจนถึงการเลี้ยงอัณฑะบนชิพ (Testis-on-chip) การพัฒนาเทคโนโลยีจำลองแบบการสร้างอสุจิในหลอดทดลองก็ยังเป็นความท้าทายอย่างที่สุดสำหรับนักวิทยาศาสตร์
และนั่นคือสาเหตุที่ทำให้นิตเซนเลือกที่จะทะลวงฟันแก้ปัญหา พัฒนาวิธีการเพาะเลี้ยงออร์แกนอยด์อัณฑะ (หรือถ้าจะเรียกว่าอัณฑะจิ๋วก็คงไม่ผิด) ขึ้นมาให้ได้ในหลอดทดลอง
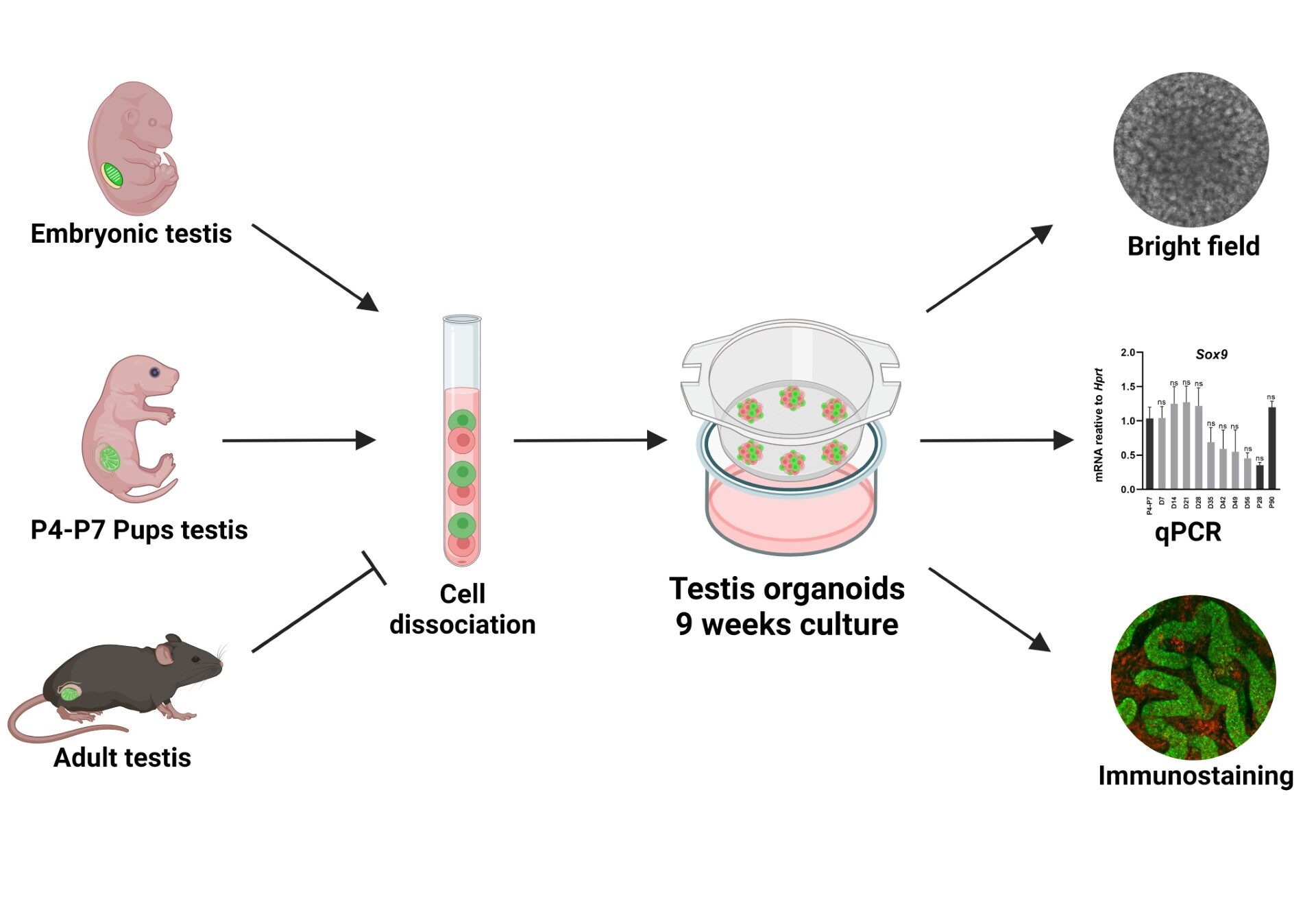
นิตเซนและทีมของเธอเริ่มกระบวนการด้วยการแยกอัณฑะจากหนูแรกเกิดและเอาไปบดปั่นจนสิ้นสภาพหลุดออกมาเป็นเซลล์เดี่ยวๆ หลังจากนั้นก็นำเอาเซลล์ที่ได้ไปเพาะเลี้ยงไว้ในจานเพาะเลี้ยงแบบหลุมกรอง (transwell) ในเซลล์อยู่ปริ่มๆ ตรงที่ระดับรอยต่อของน้ำและอากาศพอดิบพอดี
และด้วยเทคนิคการเพาะเลี้ยงแบบไม่เหมือนใคร เซลล์อัณฑะที่เธอเลี้ยงไว้นั้นจึงเติบโตออกมาได้แบบที่คนอื่นไม่เคยเจอ
แทนที่จะเป็นก้อนกระจุกเซลล์กลมเหมือนกับที่พบในการเพาะเลี้ยงออร์แกนอยด์ทั่วไป
เซลล์อัณฑะของเธอประกอบตัวเป็นท่อ และเมื่อศึกษาโครงสร้างและองค์ประกอบภายในท่ออย่างละเอียด เธอก็พบว่าภายในของออร์แกนอยด์ท่ออัณฑะที่เธอได้มานั้นมีโครงสร้างลักษณะที่เหมือนกันกับที่พบในท่อเซมินิเฟอรัส (seminiferous tubules) ที่เป็นโครงสร้างหลักของอัณฑะจริงๆ แทบไม่ผิดเพี้ยน
นอกจากนี้ เธอยังพบเซลล์สำคัญหลายชนิดที่พบในอัณฑะจริงๆ อย่างเซลล์เลย์ดิก (Leydig cell) และเซลล์เซอโทไล (Sertoli cell) ที่ควบคุมการสร้างฮอร์โมนในอวัยวะเพศและมีบทบาทในกระบวนการสร้างอสุจิอีกด้วย
ที่สำคัญ ออร์แกนอยด์ท่ออัณฑะของเธอนั้นสามารถคงสภาพอยู่ในสภาวะเพาะเลี้ยงได้นานถึงกว่าสองเดือน ซึ่งเป็นเวลาที่เหลือเฟือสำหรับสร้างอสุจิและการหลั่งฮอร์โมนที่จำเป็นเพื่อควบคุมการทำงานของอัณฑะ อาทิ ฮอร์โมนเทสโทสเทอโรน ซึ่งโดยปกติแล้ว กระบวนการพวกนี้จะใช้เวลาทั้งสิ้นราวๆ 34 วัน
อย่างไรก็ตาม ในเวลานี้ นิตเซนยังไม่สามารถยืนยันได้ว่าออร์แกนอยด์อัณฑะที่เธอเลี้ยงขึ้นมานั้นจะสามารถผลิตอสุจิและฮอร์โมนเทสโทสเทอโรนได้จริง
แต่จากผลการทดลองเบื้องต้น ทีมของเธอค่อนข้างมั่นใจว่าเซลล์ในท่อออร์แกนอยด์ของเธอน่าจะมีการแบ่งเซลล์แบบ “ไมโอสิส” เพื่อสร้างเซลล์สืบพันธุ์อีกด้วย
แม้ว่าจะยังไม่รู้ว่าอัณฑะเพาะเลี้ยงของนิตเซนจะทำงานได้สมบูรณ์แบบสมควรที่จะเป็นอัณฑะหรือไม่ แต่ทุกคนในทีมของเธอก็ยังเชื่อว่าเทคโนโลยีที่พวกเธอพัฒนาขึ้นมานี้จะสร้างคุณูปการอย่างมหาศาลให้กับมวลมนุษยชาติ โดยเฉพาะอย่างยิ่งเพื่อให้เราสามารถเข้าใจต้นเหตุของความผิดปกติของการสร้างอสุจิในผู้มีบุตรยากได้
“คลินิกเจริญพันธุ์สามารถที่จะจำแนกปัญหาที่ส่งผลให้เกิดการเป็นหมันในชายได้ อย่างเช่น จำนวนอสุจิน้อย หรืออสุจิพิการ กระนั้น เราก็ยังไม่เข้าใจอย่างถ่องแท้ว่าต้นเหตุที่แท้จริงของความผิดปกติพวกนั้นคืออะไร การกลายพันธุ์แบบใดในจีโนมที่ทำให้เกิดภาวะโรคแบบนั้น หรืออัณฑะทำงานผิดเพี้ยนไปอย่างไรถึงส่งผลให้ท่อสูญเสียความสามารถในการสร้างและเก็บอสุจิเอาไว้” นิตเซนกล่าว
แน่นอนถ้าท่ออัณฑะจิ๋วของเธอสามารถจำลองกระบวนการสร้างอสุจิทั้งหมดได้ โอกาสที่เราจะศึกษาและทำความเข้าใจกระบวนการอันซับซ้อนของการสร้างเซลล์สืบพันธุ์ได้อย่างถ่องแท้ก็คงอยู่ไม่ไกล
ในอนาคต นิตเซนมีแผนที่จะเดินหน้าทดลองเทคนิคของเธอต่อในมนุษย์ ซึ่งถ้าสำเร็จ ก็ต้องบอกว่าอาจจะเป็นหนึ่งในเทคโนโลยีแห่งความหวังที่จะมาพลิกโฉมหน้าของวงการช่วยเจริญพันธุ์ไปเลยก็เป็นได้
ยิ่งในสถานการณ์ปัจจุบัน ทั้งมลพิษ ทั้ง PM 2.5 อัตราคนเกิดก็ลดลง อย่างนี้ ต้องช่วยกันลุ้นให้สำเร็จไวๆ สำหรับเทคโนโลยีนี้…
ใครจะรู้สักวัน “อัณฑะจิ๋วอาจจะกู้โลกก็เป็นได้”
สะดวก ฉับไว คุ้มค่า สมัครสมาชิกนิตยสารมติชนสุดสัปดาห์ได้ที่นี่https://t.co/KYFMEpsHWj
— MatichonWeekly มติชนสุดสัปดาห์ (@matichonweekly) July 27, 2022