| ที่มา | มติชนสุดสัปดาห์ ฉบับวันที่ 23 - 29 เมษายน 2564 |
|---|---|
| คอลัมน์ | ทะลุกรอบ |
| เผยแพร่ |
ทะลุกรอบ
ป๋วย อุ่นใจ
ปฏิบัติการสร้างอาวุธอสรพิษ
บ่ายวันหนึ่ง ที่ห้องแล็บอณูชีววิทยาในมหาวิทยาลัยยูเทรซต์ (Utrecht University) ฉากในจินตนาการของหนังจูราสสิกปาร์ก จูราสสิกเวิร์ลด์ ดูเหมือนจะกลับกลายเป็นความจริง
ใบมีดผ่าตัดกำลังจรดอย่างแผ่วเบาเหนือปากของตัวอ่อนอสรพิษที่ถูกแคะออกมาจากไข่อย่างทะนุถนอม
ต่อมพิษขนาดจิ๋วถูกผ่าแยกและสับจนละเอียดเป็นชิ้นเล็กชิ้นน้อยก่อนที่จะนำไปเลี้ยงต่อในจานเพาะเลี้ยงเซลล์ ที่เติมเต็มเพียบพร้อมไปด้วยอาหารเพาะเลี้ยง ฮอร์โมน ซีรัม โปรตีนเร่งการเจริญ องค์ประกอบของโครงร่างภายนอกเซลล์ และสารต่างๆ มากมายที่เกี่ยวข้องกับการควบคุมการเจริญของเซลล์สัตว์
สารเหล่านี้เป็นส่วนผสมสำหรับเพาะเลี้ยงเซลล์สัตว์เลี้ยงลูกด้วยนม อย่างเซลล์มนุษย์

ห้องปฏิบัติการของฮานส์ ถือเป็นหนึ่งในห้องแล็บชั้นนำของโลกทางด้านสเต็มเซลล์และการเพาะเลี้ยงอวัยวะ เขาคือหนึ่งในผู้บุกเบิกการเพาะเลี้ยงออร์แกนอยด์ (organoid) หรืออวัยวะเวอร์ชั่นจิ๋ว (miniorgan)
ออร์แกนอยด์ส่วนใหญ่จะมีเซลล์และโครงสร้างเหมือนๆ กับที่พบในอวัยวะจริง แต่อาจจะยังไม่ถึงขนาดพัฒนาไปเป็นอวัยวะที่ทำงานได้
ทว่าออร์แกนอยด์ก็ยังมีประโยชน์อย่างมหาศาลในการศึกษาการทำงานและบทบาทของเซลล์ชนิดต่างๆ ที่พบในอวัยวะหลายๆ ชนิด
“ไม่มีใครรู้อะไรเลยเกี่ยวกับสเต็มเซลล์ในงู” ฮานส์ เคลเวอร์ส์ (Hans Clevers) นักอณูชีววิทยา จากสถาบันวิจัยฮิวเบรซต์ มหาวิทยาลัยยูเทรซต์ ประเทศเนเธอร์แลนด์กล่าว “เรายังไม่รู้เลยว่ามันจะเป็นไปได้หรือเปล่า”
ฮานส์เปิดเผยว่างานนี้ทำขึ้นมาจากความสนใจของนักศึกษาล้วนๆ ซึ่งนักศึกษาปริญญาเอกสามคนของฮานส์ที่เป็นตัวตั้งตัวตีในการทำงานนี้ก็คือ โยริก โพสต์ (Yorick Post) เจนส์ พุสชฮอฟ (Jens Puschhof) และโจเอป บิวเมอร์ (Joep Beumer)
“ถ้าเราบอกฮานส์ตั้งแต่แรก เราอาจจะไม่ได้ทำงานนี้ก็ได้” เจนส์ พุสชฮอฟ หนึ่งในทีมนักศึกษากล่าว
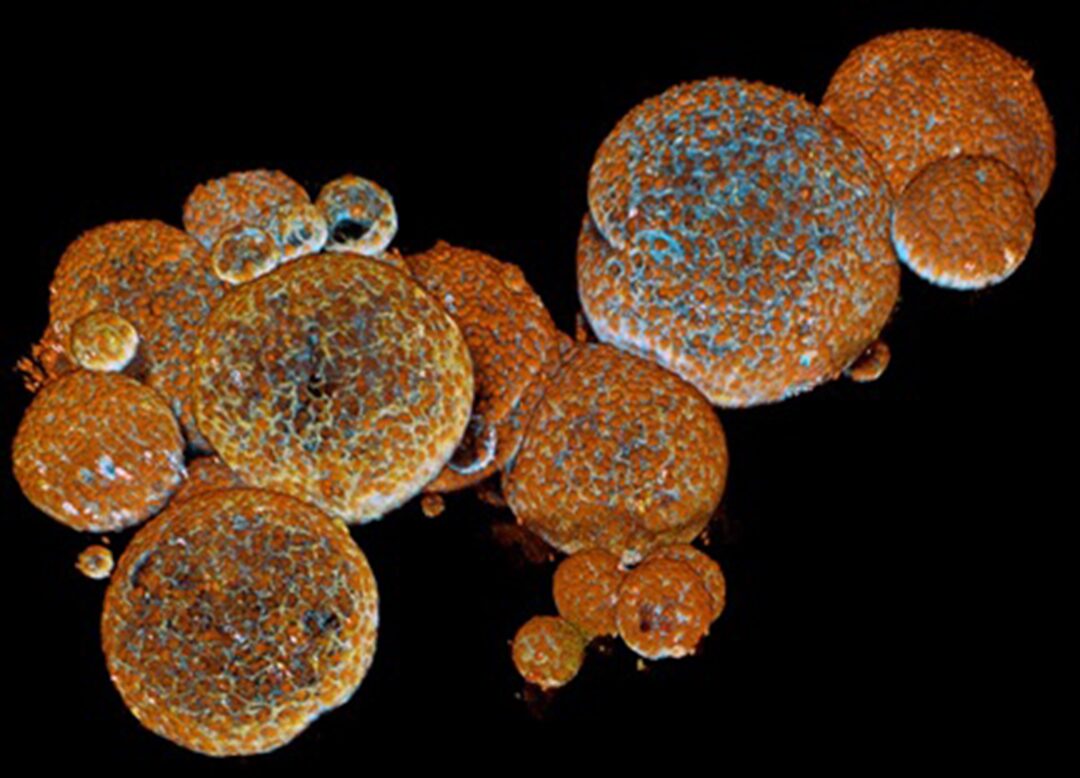
แต่ปรากฏว่ามันเวิร์ก เวลาผ่านไป 1 สัปดาห์ เซลล์ต่อมพิษงูเริ่มแบ่งเซลล์และจับตัวเป็นก้อนเนื้อเยื่อกลมๆ เล็กๆ เล็กจนแทบจะมองด้วยตาเปล่าไม่เห็น (ขนาดโดยเฉลี่ยก็ประมาณครึ่งมิลลิเมตร) เซลล์งูตอบสนองอย่างดีเยี่ยมกับสารและฮอร์โมนต่างๆ ที่ให้เข้าไป แม้ว่าจะที่จริงแล้ว จะเป็นสูตรที่ใช้กับเซลล์สัตว์เลี้ยงลูกด้วยนม อย่างเซลล์มนุษย์ก็ตาม
ซึ่งเป็นเรื่องที่น่าดีใจเป็นอย่างมากเพราะขนาดงูที่เป็นสัตว์เลี้อยคลาน ก็ยังเอาสารของคนมาใช้ได้ ก็เป็นไปได้ว่าสูตรอาหารในแบบเดียวกันนี้ก็น่าจะเพียงพอแล้วที่จะช่วยเติมเต็มกระบวนการทางชีววิทยาที่จำเป็นในการเจริญเติบโตของเซลล์สัตว์พวกเอ็กโซติก (exotic) ได้ และก็น่าจะใช้ได้ผลเหมือนๆ กันในการเพาะเลี้ยงเซลล์ของสัตว์มีกระดูกสันหลังแบบอื่นๆ อย่างปลา กิ้งก่า จระเข้ หรือแม้แต่ตัวเงินตัวทองก็น่าจะพอเลี้ยงได้
สิ่งเดียวที่ต่างไปก็คืออุณหภูมิที่ใช้ในการเลี้ยงออร์แกนอยด์ พวกเขาพบว่าเซลล์ต่อมพิษงูโตได้ดีที่อุณหภูมิราวๆ 32 องศาเซลเซียส แทนที่จะเป็น 37 องศาเซลเซียส ซึ่งก็ไม่น่าแปลกใจมากนักเพราะงูเป็นสัตว์เลือดเย็น
หลังจากที่พวกเขาเปลี่ยนสูตรอาหารเพาะเลี้ยงในจานเลี้ยงจานหนึ่ง เซลล์ในก้อนเนื้อเยื่อกลมพวกนั้นก็เริ่มเปลี่ยนสภาพกลายเป็นเซลล์เยื่อบุที่เริ่มสร้างพิษออกมา
ก้อนออร์แกนอยด์กลมๆ ที่จากเซลล์ต่อมพิษงูเริ่มบวมออกอย่างช้าๆ เซลล์ในก้อนเนื้อขนาดจิ๋วนั้นค่อยๆ หลั่งพิษงูออกมาสะสมอยู่ข้างใน
นี่เป็นเรื่องที่น่าว้าวมากสำหรับวงการชีววิทยา
พวกเขาตื่นเต้นมาก ทีมวิจัยเริ่มศึกษาการแสดงออกของยีนในออร์แกนอยด์ต่อมพิษงู ปรากฏว่าต่อมพิษจิ๋วที่พวกเขาเพาะเลี้ยงได้นั้น มีการแสดงออกของยีนเหมือนกันเป๊ะกับที่พบในต่อมพิษของงูพิษจริงๆ
ที่เด็ดกว่านั้นคือพิษที่พวกมันผลิตออกมาได้นั้น มีองค์ประกอบที่แทบจะถอดแบบออกมาจากพิษงูจริงๆ ในธรรมชาติ
พิษงูจากจานเพาะ มีพิษไม่ต่างพิษจริง แค่ใส่ลงไปนิดเดียวก็สามารถสังหารเซลล์กล้ามเนื้อและเซลล์ประสาทในจานเพาะเลี้ยงที่พวกเขาเอามาทดสอบจนแทบไม่เหลือซาก
พวกเขาเริ่มติดตามการแสดงออกในระดับยีน แรกเริ่มเดิมที เรายังไม่รู้เซลล์แต่ละชนิดในต่อมพิษมีส่วนร่วมอย่างไรบ้างในการสร้างพิษงูที่เป็นสารผสมที่ซับซ้อนประกอบไปด้วยเพปไทด์สายสั้นๆ และโปรตีนอีกนับร้อยนับพัน
แต่เทคโนโลยีออร์แกนอยด์ทำให้พวกเขาสามารถติดตามแทบทุกกระบวนการทางชีวเคมีในการสร้างพิษได้ในระดับเซลล์
นี่คือเทคโนโลยีที่จะนำพาให้เราสามารถทำความเข้าใจกับกระบวนการที่ซับซ้อนในการสร้างพิษงูในระดับเซลล์ได้อย่างถ่องแท้
ทีมวิจัยของฮานส์พบว่าเซลล์แต่ละชนิดในต่อมพิษงูจะทำหน้าที่ในการสร้างโปรตีนพิษต่างชนิดกัน
และเมื่อเขาปรับสูตรอาหาร เซลล์บางชนิดก็จะเจริญได้ดีกว่า และจะหลั่งพิษบางชนิดออกมาได้มากกว่าเซลล์ชนิดอื่นๆ
นั่นหมายความว่าแค่ปรับวิธีการเลี้ยงเพียงเล็กน้อย พวกเขาก็อาจจะกำหนดชนิดของพิษที่จะสร้างได้
องค์การอนามัยโลกประมาณการว่าในแต่ละปี จะมีผู้โชคร้ายถูกงูกัดราวๆ 5 ล้านคน และอาจมีผู้เสียชีวิตมากถึงแสนคน
แน่นอนว่าไอเดียหนึ่งในการนำไปประยุกต์ต่อยอดก็คือเอาไปใช้เพื่อสร้างพิษงูขึ้นมาเพื่อเอาไปกระตุ้นการสร้างเซรุ่มแก้พิษ
แต่เดิม การสร้างเซรุ่มจะอาศัยพิษจากการรีดพิษงู และเนื่องจากองค์ประกอบของพิษงูแต่ละชนิดไม่เหมือนกัน การจะผลิตเซรุ่มต้านพิษงูชนิดใดชนิดหนึ่งจึงจำเป็นต้องได้พิษงูชนิดนั้นๆ มาก่อน
นั่นหมายความว่าผู้ผลิตเซรุ่มจะต้องหางูพิษต่างๆ มาเลี้ยงเอาไว้เพื่อรีดพิษไว้สร้างเซรุ่ม
คือถ้าต้องการสร้างเซรุ่มแก้พิษงูพิษหายาก นักวิจัยก็จะต้องส่งทีมล่างูลงไปตามล่าหางูพิษมาเก็บไว้ ซึ่งบางทีลงภาคสนามแป๊บเดียวก็หาเจอ
แต่บางที หาเท่าไรก็หาไม่เจอก็มี การผลิตเซรุ่มงูพิษหายากจึงต้องขึ้นกับทีมล่างูและดวงอยู่พอสมควร
ยิ่งไปกว่านั้น งูแต่ละตัวก็สามารถให้พิษได้อย่างจำกัด ถ้าอยากได้พิษเยอะๆ ก็ต้องไปหาจับเพิ่ม ซึ่งจะเจอหรือไม่ก็ต้องวัดดวงเอา แถมยังต้องเสี่ยงชีวิตไปตามจับมันมากล่อมเกลี้ยงเลี้ยงดูอีก
แต่ถ้าเทคโนโลยีออร์แกนอยด์สามารถช่วยให้พวกเขาเพาะเลี้ยงต่อมพิษงูและผลิตพิษงูที่พวกเขาต้องการได้ในหลอดทดลอง ใครเจองูพิษตาย ก็รีบส่งมาแยกต่อมพิษแล้วลงจานเพาะเลี้ยง เพาะให้เป็นออร์แกนอยด์ แล้วแช่แข็งเก็บไว้เป็นแต่ละชนิด ทำเป็นธนาคารออร์แกนอยด์ต่อมพิษ หรือ biobank ที่ต้องการพิษงูอะไรก็ไปเบิกออร์แกนอยด์ออกมาเลี้ยงผลิตพิษได้ทันที พร้อมให้บริการ
เลี้ยงแต่เซลล์ ไม่ต้องจับงู ไม่ต้องเลี้ยงงู ไม่ต้องเจอกับงู ไม่ต้องเสี่ยงโดนกัด
และอยากได้เมื่อไรก็ผลิตได้เลยเท่าที่ต้องการ
ถ้าผลักดันเทคโนโลยีนี้ไปถึงจุดนั้นได้ กระบวนการผลิตเซรุ่มแก้พิษอาจจะถูกพลิกโฉมไปตลอดกาล
ยิ่งไปกว่านั้น เนื่องจากพิษงูมีสารที่เป็นองค์ประกอบนับร้อยนับพัน จึงมีการนำสารสกัดจากพิษงูมาใช้เป็นเข้าตำรับเป็นยาอยู่พอสมควรทั้งยาแก้ปวด ยาความดันโลหิตสูง หรือแม้แต่ยาต้านมะเร็ง ซึ่งถ้าหากว่ามีการสร้างธนาคารต่อมพิษขึ้นมาจริงๆ ก็อาจจะเป็นแหล่งค้นคว้าหายาใหม่จากพิษงูที่อาจจะนำมาใช้ประโยชน์ในทางการแพทย์ได้อีกมากมายมหาศาล
ตอนนี้ ทีมยูเทรซต์กำลังเดินหน้าเก็บสะสมต่อมพิษจากงูและสัตว์มีพิษอื่นๆ อีกห้าสิบชนิด โดยมีความร่วมมือกับฟรีก วองก์ (Freek Vonk) ผู้เชี่ยวชาญด้านสัตว์เลื้อยคลานจากศูนย์ความหลากหลายทางชีวภาพแนชูรัลลิส (Naturalis Biodiversity Center) ในเนเธอร์แลนด์ เพื่อศึกษากลไกการสร้างพิษชนิดต่างๆ ภายในห้องปฏิบัติการ
“มันเป็นเรื่องที่น่าตื่นเต้นมากที่ได้เห็นว่าสิ่งที่เกิดขึ้นจากความอยากรู้ของพวกเราเรื่องเอาศักยภาพในการเอาต่อมพิษงูมาเลี้ยงเป็นออร์แกนอยด์ได้แปรสภาพไปเป็นเทคโนโลยีที่มีแนวทางและโอกาสในการประยุกต์ใช้ที่หลากหลายที่จะส่งผลกระทบต่อความเป็นอยู่ของคน”
โยริก โพสต์ กล่าวด้วยสายตาที่เป็นประกาย
งานนี้ แม้จะน่าประทับใจเพราะเป็นงานที่มีแนวคิดใหม่ ส่งผลกระทบสูง เรียกว่าอาจจะเปิดศักราชใหม่แห่งวงการอุตสาหกรรมเซรุ่มต้านพิษไปเลย
แต่สำหรับผม สิ่งที่น่าประทับใจที่สุดไม่ใช่ตัวงาน แต่เป็นระบบการศึกษาที่พร้อมจะช่วยสร้างและบ่มเพาะผู้เชี่ยวชาญตัวจริงที่สนุกกับงานวิจัยและพร้อมจะออกมาสู่ตลาดแรงงานด้วยแรงบันดาลใจที่เต็มเปี่ยม เป็นกำลังคนคุณภาพส่งคืนให้กับสังคม
จากที่มีโอกาสได้คลุกคลีอยู่ในแวดวงการศึกษาในเมืองไทยมาพัก ผมเชื่อนะครับว่า ถ้าประเทศเรามีระบบห้องปฏิบัติการและระบบการสนับสนุนงานวิจัยในระดับเดียวกัน
เราก็น่าจะสามารถปั้นน้องๆ เป็นผู้เชี่ยวชาญหน้าใหม่วัยเยาว์ที่มีคุณภาพไม่แพ้น้องๆ นักศึกษาปริญญาเอกสามทหารเสือของฮานส์ได้ไม่ยากเย็น
ท้ายที่สุด ประเทศไทยในฐานะหนึ่งในประเทศที่มีความหลากหลายทางชีวภาพมากที่สุดในโลก อาจจะต้องเริ่มหันมามองกันอีกรอบว่า ถ้าเทคโนโลยีเดินไปข้างหน้าในทิศทางแบบนี้ แล้วประเทศของเราจะเดินหน้าไปต่อกันอย่างไรให้ไม่ถูกทิ้งไว้ข้างหลัง







